秋⼭芳展 医⽣物学研究所教授、檜作洋平 同助教、清⽔洋祐 同博⼠前期課程学生、禾晃和 横浜市立大学准教授らの研究チームは、大阪大学蛋白質研究所、東北大学大学院医学系研究科と共同で、細胞膜の中で働く特殊なタンパク質分解酵素RsePが基質となるタンパク質を結合した状態の立体構造を明らかにしました。本研究により、RsePの内部に取り込まれた基質タンパク質は、しっかりと固定(ヘッドロック)され、引き伸ばされた状態で切断されることが明らかになりました。切断の仕組みを詳しく調べていくことで、将来的には、細菌の感染や増殖を抑える薬剤の開発につながることが期待されます。
本研究成果は、2025年2月26日に、国際学術誌「Science Advances」に掲載されました。
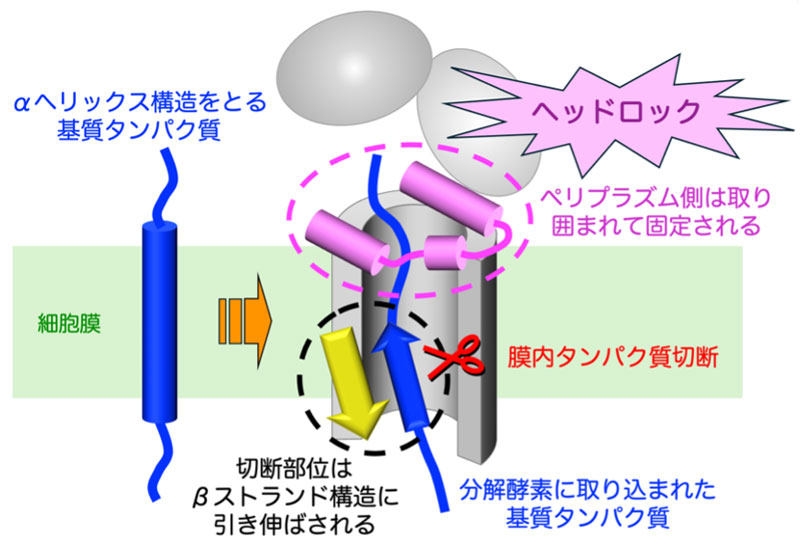
「今回の研究対象である膜内切断プロテアーゼは、本来は疎水的環境である細胞膜の内部でタンパク質の加水分解反応を行うというユニークな酵素です。この酵素は細菌からヒトまでさまざまな生物種が持っており、重要な生体プロセスの制御に関わっているものの、膜の内部に存在するという特性から、その解析は容易ではありませんでした。今回酵素と基質の複合体構造が決定され、その結合様式も明らかとなってきました。創薬基盤の基礎となるこれらの情報が得られたことで、病原菌の感染や増殖を抑えるような感染症治療薬や予防薬の開発につなげていきたいと考えています。 」(檜作洋平)
【DOI】
https://doi.org/10.1126/sciadv.adu0925
【KURENAIアクセスURL】
http://hdl.handle.net/2433/292268
【書誌情報】
Kikuko Asahi, Mika Hirose, Rie Aruga, Yosuke Shimizu, Michiko Tajiri, Tsubasa Tanaka, Yuriko Adachi, Yukari Tanaka, Mika K. Kaneko, Yukinari Kato, Satoko Akashi, Yoshinori Akiyama, Yohei Hizukuri, Takayuki Kato, Terukazu Nogi (2025). Cryo-EM structure of the bacterial intramembrane metalloprotease RseP in the substrate-bound state. Science Advances, 11, 9, eadu0925.





