2011年9月2日

左から小松教授、柳原研究員
小松賢志 放射線生物研究センター教授、柳原啓見 同研究員らの研究成果が、科学誌「Molecular Cell」電子版に掲載されました
【論文情報】
Molecular Cell, 2011年9月2日号
NBS1 Recruits RAD18 via a RAD6-Like Domain and Regulates Pol η-dependent Translesion DNA Synthesis
H. Yanagihara, J. Kobayashi, S. Tateishi, A. Kato, S. Matsuura, H. Tauchi, K. Yamada, J. Takezawa, K. Sugasawa, C. Masutani, F. Hanaoka, C. M. Weemaes, T. Mori, L. Zou, K. Komatsu
背景
ナイミーヘン症候群は、コリー・ウイーマ(ナイミーヘン大学)によって1981年に報告された、電離放射線感受性や高発がん性を特徴とするヒト遺伝病である(図1)。1998年に小松研究室を含めて、ドイツ、米国の3研究室が独立に原因遺伝子NBS1の単離に成功した(Matsuura, Nature Genet, 1998)。続いて、2002年には小松等のグループによりNBS1が、放射線照射による最も重篤なDNA損傷であるDNA二重鎖切断の再結合をおこなうこと(Tauchi, Nature, 2002)、ジャクソン等(ケンブリッジ大学)は再結合の間、細胞増殖を停止させる機能を有すること(Falck, Nature, 2005)を報告した(図2)。また、最近我々は、コンパクトに折りたたまれたDNAを再結合に先立って解きほぐすのにNBS1が必須であることを報告した(Nakamura, Mol Cell, 2011 March)。
 図1 ナイミーヘン症候群の患者 | 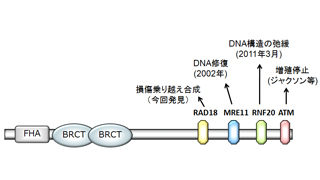 図2 NBS1蛋白構造と機能 |
色素性乾皮症バリアントは日光(紫外線)過敏症および日光暴露部位からの皮膚がんを呈するヒト遺伝病である。1999年に大阪大学の花岡ら(現学習院大学教授)により損傷乗り越え型のDNA複製酵素Pol eta(ポリメレース・イータ)が原因遺伝子として単離された(Masutani, Nature, 1999)。また、山泉ら(熊本大学、故人)のグループにより、通常のDNA複製酵素から損傷乗り越え型Pol etaへの変換にはRAD18ユビキチン酵素が必須であることが報告された(Watanabe, EMBO J, 2004)。それではRAD18が紫外線による損傷をどのようにして認識するかについては、DNA結合蛋白RPAが重要であるとする報告もあったが、矛盾点もあり未解決のままであった。
研究の概要
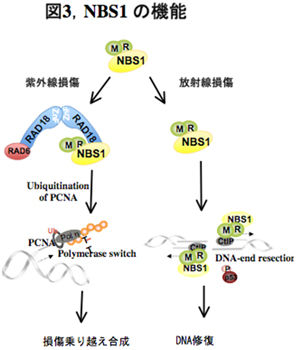
我々は、ナイミーヘン症候群患者細胞の中には放射線感受性に加えて、紫外線感受性を示す細胞があることに気づいた。解析の結果、通常RAD18ユビキチン酵素はRAD6と結合して活性化されるが、NBS1はそのRAD6と似たDNA構造をしていることが分かった。紫外線照射を受けるとNBS1がRAD6に代わってRAD18ユビキチン酵素と結合、そして紫外線による損傷部位にRAD18ユビキチン酵素をリクルートする(図3)。これにより、損傷部位で、通常のDNA複製酵素から損傷乗り越え型酵素Pol etaへの交換が起こり損傷乗りこえ合成が開始する。逆に、NBS1が欠失すると、RAD18ユビキチン酵素およびPol etaは損傷部位に集まらず、損傷乗りこえ合成が進まない。その結果として、紫外線高感受性になる。
研究の意義
放射線障害とDNA修復
生物が放射線照射をゆっくり時間をかけて受けると、一度に急に照射された場合に比べて障害が少ないことが知られている。これは、ゆっくり照射されるとその間にDNA損傷(この場合にはDNA二重鎖切断)が修復されるからである。また、放射線による少量のDNA損傷は修復できるが、1箇所に沢山の損傷が発生すると修復できない事も知られている。このように、放射線障害の発生とDNA修復とは深い関連がある。
コーデネート蛋白
放射線は、生物にとって最も重篤なDNA損傷を発生する。このため、DNA修復機構のみならず、修復期間は細胞増殖を停止させる機構など、幾つかの機能の協調的な制御が必要である。NBS1はDNA修復、細胞増殖停止、DNA構造の弛緩、そして今回発見の損傷乗りこえ合成の制御など多くの機能があることから(図2)、これらを統一的に行わせるコーデネート(指令)蛋白である可能性が高まった。
医療応用
上記のように、DNA修復は放射線障害の基礎研究として重要である。また、損傷乗り越え合成は、制がん剤のシスプラチン処理からの細胞の修復や、免疫多様性獲得のためのクラススイッチ機構に重要であることが知られている。このためコーデネート蛋白NBS1機能を阻害させる方法の開発により、放射線治療や抗癌剤の増感や免疫機能を人工的に低下させるための医療応用が期待される。
修復蛋白の起源の謎
電離放射線は1895年のレントゲンによるX線の発見から、わずか110年余の歴史しかない。それにも関わらず、発見時に既にヒトの細胞を電離放射線から防護するDNA修復機構が生命に存在していたことは驚きである。電離放射線の蛋白として知られるNBS1が紫外線(太陽光)によるDNA損傷にも機能していることを示した今回の発見は、電離放射線の修復機構の起源を探る重要な手がかりを与えると期待される。
関連リンク
- 論文は以下に掲載されております。
http://dx.doi.org/10.1016/j.molcel.2011.07.026
http://hdl.handle.net/2433/145963 (京都大学学術情報リポジトリ(KURENAI))
- 京都新聞(9月20日 7面)および日刊工業新聞(9月2日 17面)に掲載されました。

